| Глутаминовая кислота | |
|---|---|
 | |
 | |
 | |
| Общие | |
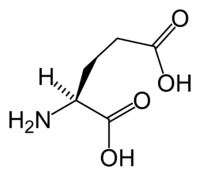
| Систематическое наименование |
2-Аминопентандиовая кислота |
| Сокращения |
Глу, Glu, E GAA,GAG |
| Традиционные названия | Аминоглутаровая кислота, глутаминовая кислота, глутамат |
| Хим. формула | C5H9NO4 |
| Рац. формула | C 40,82 %, H 6,17 %, N 9,52 %, O 43,5 % |
| Физические свойства | |
| Состояние | белый кристаллический порошок |
| Молярная масса | 147,1293 ± 0,006 г/моль |
| Плотность |
1,4601 1,538 (25° С) |
| Термические свойства | |
| Т. плав. | 160 °C |
| Т. кип. | 205 °C |
| Т. разл. | свыше 205 °C |
| Химические свойства | |
| pKa | 2,16, 4,15, 9,58 |
| Растворимость в воде | 7.5 г/л[1] |
| Изоэлектрическая точка | 3,22 |
| Классификация | |
| Рег. номер CAS | 56-86-0 |
| PubChem | 611 |
| Рег. номер EINECS | 200-293-7 |
| SMILES | |
| InChI | |
| Кодекс Алиментариус | E620 |
| ChEBI | 18237 |
| ChemSpider | 591 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Глутами́новая кислота (2-аминопентандиовая кислота) — органическое соединение, алифатическая дикарбоновая аминокислота. В живых организмах глутаминовая кислота входит в состав белков, ряда низкомолекулярных веществ и в свободном виде. Глутаминовая кислота играет важную роль в азотистом обмене.
Глутаминовая кислота также является нейромедиаторной аминокислотой, одним из важных представителей класса «возбуждающих аминокислот»[2]. Связывание глутамата со специфическими рецепторами нейронов приводит к возбуждению последних.
Глутаминовая кислота относится к группе заменимых аминокислот и играет важную роль в организме. Её содержание в организме составляет до 25% от всех аминокислот.
Физико-химические свойства
Глутаминовая кислота представляет собой белое кристаллическое вещество, плохо растворимое в воде, этаноле, нерастворимое в ацетоне и диэтиловом эфире.
Глутамат как нейромедиатор
Глутамат (соль глутаминовой кислоты) — наиболее распространённый возбуждающий нейротрансмиттер в нервной системе позвоночных[3]. В химических синапсах глутамат запасается в пресинаптических пузырьках (везикулах). Нервный импульс запускает высвобождение глутамата из пресинаптического нейрона. На постсинаптическом нейроне глутамат связывается с постсинаптическими рецепторами, такими, как, например, NMDA-рецепторы, и активирует их. Благодаря участию последних в синаптической пластичности глутамат вовлечён в такие когнитивные функции, как обучение и память[4]. Одна из форм синаптической пластичности, называемая долговременной потенциацией, имеет место в глутаматергических синапсах гиппокампа, неокортекса и в других частях головного мозга. Глутамат участвует не только в классическом проведении нервного импульса от нейрона к нейрону, но и в объёмной нейротрансмиссии, когда сигнал передаётся в соседние синапсы путём суммации глутамата, высвобожденного в соседних синапсах (так называемая экстрасинаптическая или объёмная нейротрансмиссия)[5] В дополнение к этому, глутамат играет важную роль в регуляции конусов роста и синаптогенеза в процессе развития головного мозга, как это было описано Марком Мэтсоном.
Транспортёры[6] глутамата обнаружены на нейрональных мембранах и мембранах нейроглии. Они быстро удаляют глутамат из внеклеточного пространства. При повреждении мозга или заболеваниях они могут работать в противоположном направлении, вследствие чего глутамат может накапливаться снаружи клетки. Этот процесс приводит к поступлению большого количества ионов кальция в клетку через каналы NMDA-рецепторов, что, в свою очередь, вызывает повреждение и даже гибель клетки — что получило название эксайтотоксичности. Механизмы клеточной смерти при этом включают:
- повреждение митохондрий избыточно высоким внутриклеточным кальцием,
- Glu/Ca2+-опосредованной промоцией факторов транскрипции проапоптотических генов или снижением транскрипции анти-апоптотических генов.
Эксайтотоксичность, обусловленная повышенным высвобождением глутамата или его сниженным обратным захватом, возникает при ишемическом каскаде и ассоциирована с инсультом, а также наблюдается при таких заболеваниях, как боковой амиотрофический склероз, латиризм, аутизм, некоторые формы умственной отсталости, болезнь Альцгеймера[7].[8] В противоположность этому, снижение высвобождения глутамата наблюдается при классической фенилкетонурии, приводящей к нарушению экспрессии глутаматных рецепторов[9] Глутаминовая кислота участвует в реализации эпилептического припадка. Микроинъекция глутаминовой кислоты в нейроны вызывает спонтанную деполяризацию, и этот паттерн напоминает пароксизмальную деполяризацию во время судорог. Эти изменения в эпилептическом очаге приводят к открытию вольтаж-зависимых кальциевых каналов, что снова стимулирует выброс глутамата и дальнейшую деполяризацию.
Роли глутаматной системы в настоящее время отводится большое место в патогенезе таких психических расстройств, как шизофрения и депрессия. Одной из наиболее активно изучаемых теорий этиопатогенеза шизофрении в настоящее время является гипотеза NMDA-рецепторной гипофункции: при применении антагонистов NMDA-рецепторов, таких, как фенциклидин, у здоровых добровольцев в эксперименте появляются симптомы шизофрении. В связи с этим предполагается, что гипофункция NMDA-рецепторов является одной из причин нарушений в дофаминергической передаче у больных шизофренией. Были также получены данные о том, что поражение NMDA-рецепторов иммунно-воспалительным механизмом («антиNMDA-рецепторный энцефалит») имеет клинику острой шизофрении.[источник не указан 151 день]
Глутаматные рецепторы
Существуют ионотропные и метаботропные (mGLuR1–8) глутаматные рецепторы.
Ионотропными рецепторами являются NMDA-рецепторы, AMPA-рецепторы и каинатные рецепторы.
Эндогенные лиганды глутаматных рецепторов — глутаминовая кислота и аспарагиновая кислота. Для активации NMDA рецепторов также необходим глицин. Блокаторами NMDA-рецепторов являются PCP, кетамин, и другие вещества. AMPA-рецепторы также блокируются CNQX, NBQX. Каиновая кислота является активатором каинатных рецепторов.
«Круговорот» глутамата
При наличии глюкозы в митохондриях нервных окончаний происходит дезаминирование глутамина до глутамата при помощи фермента глутаминазы. Также при аэробном окислении глюкозы глутамат обратимо синтезируется из альфа-кетоглутарата (образуется в цикле Кребса) при помощи аминотрансферазы.
Синтезированный нейроном глутамат закачивается в везикулы. Этот процесс является протон-сопряжённым транспортом. В везикулу с помощью протон-зависимой АТФазы закачиваются ионы H+. При выходе протонов по градиенту в везикулу поступают молекулы глутамата при помощи везикулярного транспортера глутамата (VGLUTs).
Глутамат выводится в синаптическую щель, откуда поступает в астроциты, там трансаминируется до глутамина. Глутамин выводится снова в синаптическую щель и только тогда захватывается нейроном. По некоторым данным, глутамат напрямую путём обратного захвата не возвращается.[10]
Роль глутамата в кислотно-щелочном балансе
Дезаминирование глутамина до глутамата при помощи фермента глутаминазы приводит к образованию аммиака, который, в свою очередь, связывается со свободным протоном и экскретируется в просвет почечного канальца, приводя к снижению ацидоза. Превращение глутамата в α-кетоглутарат также происходит с образованием аммиака. Далее кетоглутарат распадается на воду и углекислый газ. Последние, при помощи карбоангидразы через угольную кислоту, превращаются в свободный протон и гидрокарбонат. Протон экскретируется в просвет почечного канальца за счёт котранспорта с ионом натрия, а бикарбонат попадает в плазму.
Глутаматергическая система
В ЦНС находится порядка 106 глутаматергических нейронов. Тела нейронов лежат в коре головного мозга, обонятельной луковице, гиппокампе, чёрной субстанции, мозжечке. В спинном мозге — в первичных афферентах дорзальных корешков.
В ГАМКергических нейронах глутамат является предшественником тормозного медиатора, гамма-аминомасляной кислоты, образующейся с помощью фермента глутаматдекарбоксилазы.
Патологии, связанные с глутаматом
Повышенное содержание глутамата в синапсах между нейронами может перевозбудить и даже убить эти клетки, что приводит к таким заболеваниям, как АЛС. Для избежания таких последствий глиальные клетки астроциты поглощают избыток глутамата. Он транспортируется в эти клетки с помощью транспортного белка GLT1, который присутствует в клеточной мембране астроцитов. Будучи поглощённым клетками астроглии, глутамат больше не приводит к повреждению нейронов.
Содержание глутамата в природе
В этом разделе не хватает ссылок на источники информации. |
Глутаминовая кислота относится к условно незаменимым аминокислотам. Глутамат в норме синтезируется организмом. Присутствие в пище свободного глутамата придаёт ей так называемый «мясной» вкус, для чего глутамат используют как усилитель вкуса.
Содержание натуральных глутаматов в пище:
| Продукт | Свободный глутамат[11][неавторитетный источник?]
(мг/100 г) |
|---|---|
| Молоко коровье | 2 |
| Сыр пармезан | 1200 |
| Яйца птицы | 23 |
| Мясо цыплёнка | 44 |
| Мясо утки | 69 |
| Говядина | 33 |
| Свинина | 23 |
| Треска | 9 |
| Макрель | 36 |
| Форель | 20 |
| Зеленый горошек | 200 |
| Кукуруза | 130 |
| Свекла | 30 |
| Морковь | 33 |
| Лук | 18 |
| Шпинат | 39 |
| Томаты | 140 |
| Зеленый перец | 32 |
В промышленных масштабах глутаминовую кислоту получают путём микробиологического синтеза. В химически чистом виде она имеет вид белых или бесцветных кристаллов без запаха, имеющих кислый вкус, в воде кристаллы растворяются плохо. Для лучшей растворимости глутаминовую кислоту превращают в соль глутамат натрия.
Применение
Фармакологический препарат глутаминовой кислоты оказывает умеренное психостимулирующее, возбуждающее и отчасти ноотропное действие.[уточнить]
Глутаминовая кислота (пищевая добавка E620) и её соли (глутамат натрия Е621, глутамат калия Е622, диглутамат кальция Е623, глутамат аммония Е624, глутамат магния Е625) используются как усилитель вкуса во многих пищевых продуктах[12].
Глутаминовую кислоту и её соли добавляют в полуфабрикаты, различные продукты быстрого приготовления, кулинарные изделия, концентраты бульонов. Она придаёт пище приятный мясной вкус.
В медицине применение глутаминовой кислоты оказывает незначительное психостимулирующее, возбуждающее и ноотропное действие, что используют в лечении ряда заболеваний нервной системы. В середине 20 века врачи рекомендовали применение глутаминовой кислоты внутрь в случае мышечно-дистрофических заболеваний. Также её назначали спортсменам с целью увеличения мышечной массы.
Глутаминовая кислота используется в качестве хирального строительного блока в органическом синтезе[13], в частности, дегидратация глутаминовой кислоты приводит к её лактаму ― пироглутаминовой кислоте (5-оксопролину), которая является ключевым предшественником в синтезах неприродных аминокислот, гетероциклических соединений, биологически активных соединений и т. д.[14],[15],[16],[17].
Примечания
- ↑ L-Glutamic acid (англ.). Chemical book.
- ↑ Moloney M. G. Excitatory amino acids. // Natural Product Reports. 2002. P. 597―616.
- ↑ Meldrum, B. S. (2000). «Glutamate as a neurotransmitter in the brain: Review of physiology and pathology». The Journal of nutrition 130 (4S Suppl): 1007S-1015S.
- ↑ McEntee, W. J.; Crook, T. H. (1993). «Glutamate: Its role in learning, memory, and the aging brain». Psychopharmacology 111 (4): 391—401. DOI:10.1007/BF02253527 PMID 7870979
- ↑ Okubo, Y.; Sekiya, H.; Namiki, S.; Sakamoto, H.; Iinuma, S.; Yamasaki, M.; Watanabe, M.; Hirose, K.; Iino, M. (2010). «Imaging extrasynaptic glutamate dynamics in the brain». Proceedings of the National Academy of Sciences 107 (14): 6526. DOI:10.1073/pnas.0913154107.
- ↑ Shigeri, Y.; Seal, R. P.; Shimamoto, K. (2004). «Molecular pharmacology of glutamate transporters, EAATs and VGLUTs». Brain Research Reviews 45 (3): 250—265. DOI:10.1016/j.brainresrev.2004.04.004 PMID 15210307
- ↑ Robert Sapolsky (2005). «Biology and Human Behavior: The Neurological Origins of Individuality, 2nd edition». The Teaching Company. «see pages 19 and 20 of Guide Book»
- ↑ Hynd, M.; Scott, H. L.; Dodd, P. R. (2004). «Glutamate-mediated excitotoxicity and neurodegeneration in Alzheimer?s disease». Neurochemistry International 45 (5): 583—595. DOI:10.1016/j.neuint.2004.03.007 PMID 15234100
- ↑ Glushakov, AV; Glushakova, O; Varshney, M; Bajpai, LK; Sumners, C; Laipis, PJ; Embury, JE; Baker, SP; Otero, DH; Dennis, DM; Seubert, CN; Martynyuk, AE (2005 Feb). «Long-term changes in glutamatergic synaptic transmission in phenylketonuria». Brain : a journal of neurology 128 (Pt 2): 300-7. DOI:10.1093/brain/awh354 PMID 15634735
- ↑ Ашмарин И. П., Ещенко Н. Д., Каразеева Е. П. Нейрохимия в таблицах и схемах. — М.: «Экзамен», 2007
- ↑ If MSG is so bad for you, why doesn’t everyone in Asia have a headache? | Life and style | The Observer
- ↑ Садовникова М. С., Беликов В. М. Пути применения аминокислот в промышленности. //Успехи химии. 1978. Т. 47. Вып. 2. С. 357―383.
- ↑ Coppola G. M., Schuster H. F., Asymmetric synthesis. Construction of chiral moleculs using amino acids, A Wiley-Interscience Publication, New York, Chichester, Brisbane, Toronto, Singapore, 1987.
- ↑ Smith M. B. Pyroglutamte as a Chiral Template for the Synthesis of Alkaloids. Chapter 4 in Alkaloids: Chemical and Biological Perspectives. Vol. 12. Ed. by Pelletier S. W. Elsevier, 1998. P. 229―287.
- ↑ Nájera C., Yus M. Pyroglutamic acid: a versatile building block in asymmetric synthesis. //Tetrahedron: Asymmetry. 1999. V. 10. P. 2245―2303.
- ↑ Panday S. K., Prasad J., Dikshit D. K. Pyroglutamic acid: a unique chiral synthon. // Tetrahedron: Asymmetry. 2009. V. 20. P. 1581―1632.
- ↑ A. Stefanucci, E. Novellino, R. Costante, and A. Mollica. PYROGLUTAMIC ACID DERIVATIVES: BUILDING BLOCKS FOR DRUG DISCOVERY // HETEROCYCLES, 2014, V. 89, No. 8, pp. 1801―1825.
См. также
Ссылки
- Диффузная внесинаптическая нейропередача посредством глутамата и ГАМК.
- Рубцов П. П. Глютаминовая кислота // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Дубынин В. Глутамат. ИД «ПостНаука» (7 октября 2016). — лекция о передаче сенсорики, NMDA-рецепторах и свойствах глутаминовой кислоты. Проверено 21 ноября 2016.
- USDA.Glutamic acid
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .